 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
XV. 2. Електродна поляризація
Протікання струму через розчин завжди супроводжується виникненням між електродами деякої різниці потенціалів, що діє проти ЕРС, яка накладена ззовні. Це явище одержало назву поляризації.
Якщо електрохімічна система є електролізером (електрохімічною ванною), то напруга на ній при даній силі струму буде більша від оборотної ЕРС тієї самої системи ЕВ(j)>Е, і навпаки, якщо електрохімічна система генерує струм, тобто є хімічним джерелом струму – гальванічним елементом чи акумулятором, то його зовнішня напруга буде менша, ніж оборотна ЕРС Еел(j) < E. При накладанні струму потенціал кожного з двох електродів, що входять до електрохімічної системи, змінюється в напрямі, який збільшує напругу на ванні і знижує її на елементі.
Різниця між потенціалом електрода під струмом і його рівноважним потенціалом називається електродною поляризацією.
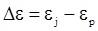 (ХV.2.1)
(ХV.2.1)
Електродна поляризація є функцією густини струму: чим вище густина струму, тим більше значення поляризації. Якщо потенціал стає більш негативним, поляризацію називають катодною, якщо більш позитивним – анодною. Вивчення кінетичних закономірностей та характеру електродних реакцій здійснюють на підставі аналізу залежностей ЕІ – І; ε – j; lg j – η; ΔE – I, які називаються також поляризаційними кривими.
Будь-який електродний процес є складною гетерогенною реакцією, що складається з ряду послідовних стадій. Це уявлення справедливе і для електрохімічної реакції. Виникнення електродної поляризації пов’язане таким чином безпосередньо з тією стадією, яка визначає швидкість процесу. Якщо відома природа лімітуючої стадії, то замість терміну “поляризація” використовується, як правило, термін “перенапруга”. Якщо найбільш повільною стадією є транспорт реагуючої речовини до електрода або продукту електрохімічної реакції від нього, то перенапруга називається дифузійною (ηД). Коли найбільш повільно протікає розряд або іонізація, виникає електрохімічна перенапруга, яка називається також перенапругою (електронного) переходу (ηЕ). Гальмування, що відбувається внаслідок фазового перетворення (утворення або руйнування кристалічної решітки, виділення бульбашок газу), або сповільненого протікання хімічної реакції, що передує (або протікає після) електрохімічної стадії, викликає виникнення відповідно фазової (ηФ) або реакційної (хімічної) (ηР) перенапруги. Кожний вид перенапруги обумовлений специфічним механізмом її появи і описується власними кінетичними рівняннями. В загальному вигляді електродна поляризація рівна сумі всіх видів перенапруги:
 (ХV.2.2)
(ХV.2.2)
Проте при конкретних електрохімічних процесах домінуюче значення може мати одна із видів перенапруги, яка і визначає поляризацію процесу в цілому.
Якщо при зміні умов протікання електродного процесу, наприклад, при підвищенні температури, швидкість лімітуючої стадії зростає, то потенціал електроду знижується. Це зниження потенціалу називається деполяризацією.
Значення поляризаційних явищ при практичному використанні нерівноважних електрохімічних систем дуже велике. Потенціали поляризованих електродів визначають напругу на електролізері і на клемах хімічного джерела струму, а значить, і енергетичні характеристики електрохімічних систем. При виборі оптимальних умов проведення електрохімічних реакцій необхідно враховувати природу і величину перенапруги, оскільки вони визначають багато характеристик процесу, наприклад, структуру катодних металічних осадів, перехід у продукт домішок і інше. Вияснення природи найбільш сповільненої стадії електродного процесу, встановлення виду перенапруги є головними завданнями електрохімічної кінетики.
Поиск по сайту: