 |
АвтоАвтоматизацияАрхитектураАстрономияАудитБиологияБухгалтерияВоенное делоГенетикаГеографияГеологияГосударствоДомДругоеЖурналистика и СМИИзобретательствоИностранные языкиИнформатикаИскусствоИсторияКомпьютерыКулинарияКультураЛексикологияЛитератураЛогикаМаркетингМатематикаМашиностроениеМедицинаМенеджментМеталлы и СваркаМеханикаМузыкаНаселениеОбразованиеОхрана безопасности жизниОхрана ТрудаПедагогикаПолитикаПравоПриборостроениеПрограммированиеПроизводствоПромышленностьПсихологияРадиоРегилияСвязьСоциологияСпортСтандартизацияСтроительствоТехнологииТорговляТуризмФизикаФизиологияФилософияФинансыХимияХозяйствоЦеннообразованиеЧерчениеЭкологияЭконометрикаЭкономикаЭлектроникаЮриспунденкция
Основы технологии этанола
Этапол, или этиловый спирт (СН3СН2ОH) является бесцветной жидкостью со жгучим вкусом и характерным запахом, имеет температуру плавления 114,5 °С, температуру кипения — 78,4 °С. Его плотность 0,794 г/см3, он растворяется в воде и органических растворителях. С водой этанол образует азе-отропную смесь, содержащую 95,6 % спирта, которая кипит при постоянной температуре 78,1 °С. Этанол обладает наркотическим действием, его предельно допустимая концентрация равна 1 г/м3. Длительное воздействие этанола на организм человека вызывает тяжелые заболевания нервной системы, печени и других органов.
Этанол известен человеку с древности, однако первые упоминания о нем относятся к VIII в. В XI—XII вв. этанол получали ректификацией виноградного вина, с XII в. его начали применять в медицине. Метод получения водного раствора этанола из картофеля впервые описал в 1682 г. И. Бехер, немецкий химик и врач. Элементный состав этанола установил французский химик А.Л. Лавуазье. В 60-х гг. XIX в. Д.И. Менделеев детально исследовал систему «этанол—вода» и использовал затем полученные данные для разработки гидратной теории; им же был установлен и оптимальный состав русской водки.
В качестве основного сырья для промышленного производства этанола используются газ этилен C2H4, древесина, зерно злаковых (в основном рожь), крахмал, картофель и сульфитные щелока. На рис. 11.3 показано применение этого сырья при получении этанола.
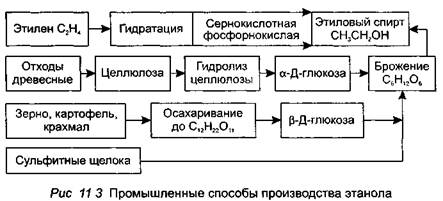
В зависимости от вида сырья выход спирта составляет (в литрах на 1 т исходного сырья): 740 для этилена; 93—117 для картофеля; 185— 361 для зерна; 160 —200 для древесины;
90—110 для сульфитных щелоков (в пересчете на 1 т древесины). Из древесины и сульфитных щелоков, кроме этанола, получают дрожжи, фурфурол, лигнин, лигносульфонаты и гипс. При всех вариантах биохимического метода производства этанола (кроме гидратации) выделяется оксид углерода (СО2).
Рассмотрим технологию получения этилового спирта прямой гидратацией в присутствии фосфорной кислоты, служащей катализатором. Основное сырье для получения этанола этим методом — этилен, выделяемый из пирогаза (продукт пиролиза низкооктанового бензина), газов нефтепереработки и попутных газов, из этиленовых фракций обратного коксового газа, а также полученного пиролизом этана.
Процесс гидратации представляет собой экзотермическую равновесную реакцию:
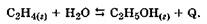
Для того, чтобы равновесие сместилось в сторону получения спирта, необходимо понижение температуры и повышение давления, однако ниже 280 °С скорость гидратации очень мала, а применение давления свыше 80-105 Па экономически нерентабельно, поэтому на практике применяют катализатор.
В качестве катализатора используется фосфорная кислота, нанесенная на широкопористые носители: кизельгур, силика-гель, алюмосиликаты. Наличие пор облегчает диффузию и увеличивает поверхность соприкосновения реагентов с фосфорной кислотой, находящейся в виде пленки на зернах твердых носителей. Таким образом, при формально твердом катализаторе катализ протекает фактически в жидкой фазе и зависит от концентрации кислоты. Концентрация кислоты в свою очередь зависит от парциального давления паров воды и температуры в системе. Например, при давлении паров воды 27,5 105 Па концентрация кислоты при 280 ° С составляет 83 % (при более низкой концентрации резко снижается активность катализатора), а при 290 °С — 85 %.
Оптимальными условиями взаимодействия газообразного этилена С2Н4 и водяных паров являются: температура 280— 290 °С; давление 70 • 105—80 • 105 Па; концентрация этилена в циркулирующем газе 80—85 % (об.); молярное отношение воды к этилену 0,6—0,75: 1; концентрация фосфорной кислоты на поверхности катализатора не ниже 83 %; объемная скорость 1800—2500 ч-1.
Соблюдение этих условий позволяет получать водноспирто-вой раствор с концентрацией спирта 15—16 % при конверсии этилена за один проход 4—5 %. Полезное использование этиле-
на на этой установке составляет 95 %. Остальные 5 % этилена расходуются на образования диэтилового эфира (2 %), ацеталь-дегида (1 %), димеров и полимеров (2 %).
В целом технологическая схема прямой гидратации этилена (рис. 11.4) включает несколько непрерывно протекающих операций:
• приготовление исходной парогазовой смеси;
• гидратацию этилена в гидраторе (реакторе);
• нейтрализацию паров продуктов, образующихся в результате реакции;
• рекуперацию тепла рециркулирующих потоков;
• очистку циркулирующего газа.

Смесь сжатых компрессором этилена, циркуляционного газа и паров воды нагревается до 280 ° С и поступает в контактный аппарат-гидратор (цилиндрическая колонна диаметром 2,5 м, высотой 10 м, футерованная изнутри красной медью), заполненный катализатором на высоту 8,5 м. Парогазовая смесь после гидратора нейтрализуется щелочью и проходит теплообменник-рекуператор, в котором отдает свое тепло поступающей исходной смеси. Образующийся в рекуператоре конденсат (водный раствор спирта) очищается от непрореагировавшего этилена, который затем снова в виде циркуляционного газа возвращается в процесс, а водный раствор спирта передается на очистку и ректификацию.
При наличии вблизи установки гидратации ТЭЦ парогазовую смесь готовят путем смешивания этилена с перегретым паром высокого давления (=70 • 105 Па).
На изготовление 1 т этилового спирта расходуется 0,685 т этилена, 5,6 кг фосфорной (100 %) кислоты, 2 кг носителя,
16 кг гидрооксида натрия NaOH. Срок службы катализатора около 600 ч, дальше его не эксплуатируют из-за осаждения на поверхности носителя смолистых веществ.
Контрольные вопросы
1. Что представляет собой пищевая промышленность? С какими сферами общественного производства она связана?
2. Охарактеризуйте основные направления научно-технологического прогресса в пищевой промышленности.
3. Охарактеризуйте технологические особенности пищевой промышленности.
4. Как классифицируются важнейшие процессы пищевой промышленности?
5. На какие группы подразделяют технологические процессы пищевых производств с учетом сути явлений, происходящих при производстве пищевой продукции?
6. Кратко охарактеризуйте типовые процессы пищевых производств.
7. Какие технологические процессы специфичны для пищевой
промышленности? Кратко охарактеризуйте их.
8. Кратко охарактеризуйте важнейшие технологические процессы термической обработки в пищевой промышленности.
9. Чем принципиально отличаются друг от друга стерилизация, пастеризация и тиндализация?
10. В чем заключается сущность консервирования? Какие группы процессов консервирования вам известны? Кратко охарактеризуйте их.
11. Кратко охарактеризуйте важнейшие технологические процессы консервирования, применяемые в пищевой промышленности.
12. Какие четыре группы пищевых производств различают в зависимости от общности основных методов обработки сырья? Кратко охарактеризуйте их.
13. Охарактеризуйте технологические особенности механико-теп-лофизических производств. Какие процессы лежат в их основе? Какие предприятия пищевой промышленности входят в эту группу?
14. Охарактеризуйте технологические особенности физико-химических производств. Какие процессы лежат в их основе? Какие предприятия пищевой промышленности входят в эту группу?
15. Охарактеризуйте технологические особенности бродильных производств. Какие процессы лежат в их основе? Какие предприятия пищевой промышленности входят в эту группу?
16. Охарактеризуйте технологические особенности химических производств. Какие процессы лежат в их основе? Какие предприятия пищевой промышленности входят в эту группу?
17. Опишите основы технологии мукомольного производства.
18. Опишите основы технологии свеклосахарного производства.
19. Опишите основы технологии кисломолочных продуктов.
20. Опишите основы технологии этанола.
Поиск по сайту: